Indigo - von diesem Wort ging über Jahrhunderte eine grosse Faszination aus. Indigo, das war einst der teure Farbstoff aus fernen Ländern, der den Menschen die blaue Farbe brachte, die sie überall in der Natur sahen , aber lange Zeit nicht herstellen konnten. Indigo ist auch ein Meilenstein in der Entwicklung der modernen Technischen Chemie. Auch heute ist es noch fesselnd, die Spur dieser Substanz in Kultur, Wissenschaft und Technik zu verfolgen. Der entscheidende Durchbruch zur synthetischen Herstellung von Indigo erfolgte 1890 an der ETH in Zürich. Auf der Suche nach Blau wurde als Nebenprodukt auch eines der ersten erfolgreichen Medikamente gefunden.
1. Physikalische Eigenschaften:
Der systematische Name ist 2,2‘-Biindolinyliden-3,3‘-dion (C16H10N2O2)
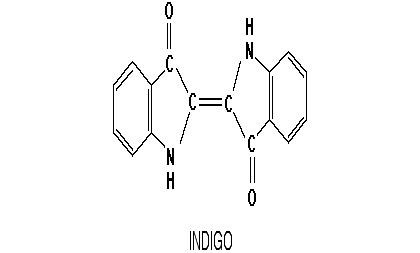
Abbildung 1: Indigo.
Das Molekulargewicht beträgt 262,26 g/mol. Die dunkelblauen Kristalle haben einen Schmelzpunkt von 390-392°C. Schon bei 170°C beginnt Indigo unter Bildung von kupferroten Prismen zu sublimieren. Indigo ist in Wasser, Ethanol, Ether und verdünnten Säuren unlöslich, in konzentrierter Schwefelsäure mit grüner, beim Erwärmen mit blauer Farbe löslich. Dabei entsteht die 5,5'-Disulfonsäure (Indigocarmin), ein wasserlöslicher Farbstoff für Wolle und Seide mit mangelhaften Licht- und Wascheigenschaften, der langezeit als Lebensmittelfarbstoff verwendet wurde. Das Absorptionsmaximum von Indigo in Ethanol liegt bei 606 nm (log e: 4,23)
Der hohe Schmelzpunkt und die schlechte Löslichkeit finden eine Erklärung in der Kristallstruktur. Aus Röntgenuntersuchungen ergibt sich, dass der Indigo im festen Zustand ein Wasserstoffbrücken-Polymer bildet; jedes Indigomolekül ist an vier umgebende Moleküle gebunden.
Durch Reduktion in Gegenwart von Alkalien mit Dithionit (Hydrosulfit), Hydroxyaceton, Zinkstaub, katalytisch angeregtem Wasserstoff oder durch biochemische Reduktion (Gärungsküpe) entsteht Leukoindigo (Indigoweiss), ein weisser kristalliner Körper, der sich in Alkalien mit gelber Farbe löst und an der Luft wieder zu Indigo oxidiert wird. Dieser Vorgang ist die Grundlage der Küpenfärberei.
Der Indigo gehört in die Klasse der Carbonylfarbstoffe. In dieser Klasse werden alle Farbstoffe, die mindestens zwei miteinander in Konjugation stehende Carbonylgruppen besitzen, zusammengefasst. Weiter gehören auch die Anthrachinonfarbstoffe in diese Gruppe.
Die Beliebtheit des Indigos bis auf den heutigen Tag ist seiner recht guten Wasch- und Lichtechtheit zu verdanken, wenn auch modernere Küpenfarbstoffe ihm deutlich überlegen sind. Auf Wolle ist seine Lichtechtheit vorzüglich. Bei längerer und intensiver Lichteinwirkung verblasst die Färbung, doch es bilden sich keine missfarbigen Abbauprodukte wie bei anderen Blaufarbstoffen.
2. Geschichte des natürlichen Indigos:
Schon in prähistorischer Zeit hat der Mensch Pelze, später Textilien und andere Gegenstände gefärbt. Als Farbstoffe dienten Naturstoffe, vor allem pflanzlichen, aber auch tierischen Ursprungs. In ägyptischen Keilschriften findet man genaue Anleitungen zur Gewinnung von Naturfarbstoffen und deren Anwendung. Doch lange Zeit fehlte das Blau. Die damaligen Menschen sahen überall blau um sich herum: am Himmel, im Wasser. Und manche Blüte und Frucht ist intensiv blau. Doch ist das eine Blau nicht greifbar, das andere nicht beständig.
Die Natur hatte zwar mehrere Möglichkeiten bereit, doch mussten sie zuerst durch spezielle Technologien gefunden und erschlossen werden. Man kann mit Recht behaupten, dass diese Prozesse die ersten biotechnologischen Verfahren darstellten.
Unabhängig voneinander wurde die Blaufärberei mit Ausnahme von Australien und dem Süden von Afrika - ausser Madagaskar - auf allen Kontinenten betrieben. Die Grundlage dazu bildeten viele Pflanzenarten, von denen zwei besonders wichtig waren.
2.1 Der Färberwaid
In unseren Breiten wächst ein Kreuzblütler mit dem lateinischen Namen Isatis tinctoria. Der deutsche Name Färberwaid zeigt, wofür diese Pflanze lange Zeit verwendet wurde. Es handelt sich um eine zweijährige Pflanze, die bis 1,2 m hoch werden kann. Die Pflanze enthält in ihren Blättern und Stengeln einen Stoff der durch geeignete Behandlung eine blaue Farbe ergibt. Dieser Färberwaid war seit der frühen Eisenzeit im europäischen Raum stark verbreitet. Eine Verwendung bei den Kelten Britanniens wird 54 v. Chr. von Julius Caesar in “De Bello Gallico” beschrieben: “Omnes vero se Britanni vitro inficiunt, quod caeruleum efficit colorem, atque hoc horribiliores sunt in pugna aspectu“ (Alle Briten malen sich mit Waid an, der wild wächst und einen blauen Farbton produziert. Das gibt ihnen in der Schlacht ein schreckliches Aussehen). Die Misserfolge der Römer auf der britischen Insel dürften aber nicht alleine auf dieser Tatsache beruhen

Abbildung 2: Isatis tinctoria
Wie andere Färberpflanzen auch, erlebte der Waid im Laufe der Jahrhunderte eine Entwicklung von der Verwendung in der bäuerlichen Hausfärberei über die Kultivierung in Hofgütern und Klostergärten bis hin zum planmässigen Anbau. Der kommerzielle Anbau von Färberwaid in Europa erlebte seine Blüte im 13. Jahrhundert. Die Hauptanbaugebiete lagen im Elsass und in Thüringen.
Der Farbstoffgehalt hängt stark vom Klima und den Bodenverhältnissen ab. Die Bauern waren nicht nur für den Anbau und die Ernte zuständig. Sie zermahlten die geernteten Blätter zu einem Brei, der zur Gärung gebracht wurde. Nach 2 Wochen, in denen die Masse mehrmals zu wenden war, formte man die sogenannten Waidkugeln oder Blaukörner, die getrocknet wurden.
Ein weiteres Verarbeiten war den Bauern verboten und durfte nur von den Waidhändlern durchgeführt werden. Diese zerkleinerten die Waidkugeln und die Masse wurde durch Anfeuchten mit Wasser und Urin einer weiteren Gärung unterworfen. Strenge Auflagen waren mit dieser stinkenden Arbeit verbunden; so durfte diese Gärung unter Androhung von schweren Strafen nicht an Festtagen durchgeführt werden. Das Endprodukt dieser nochmaligen Gärung wurde dann in Fässern, meist auf dem Landwege, über weite Strecken zu den Verbrauchern transportiert. Haupthandelsplätze für Waid waren Frankfurt, Nürnberg, Köln und Speyer.
Waid war in Europa mit Abstand der wichtigste Farbstoff des Mittelalters. So verpflichtete Karl der Grosse schon im 8. Jahrhundert alle seine Meier-Höfe zum Anbau einer gewissen Fläche Färberwaid. Dadurch sollte wohl die Eigenversorgung gesichert werden und es konnten - um in modernen Kategorien zu denken - auch Devisen gespart werden.
2.2 Indigofera tinctoria
In den tropischen und subtropischen Gebieten gibt es eine Schmetterlingsblütlerart, die Indigofera tinctoria, die gegenüber der Färberwaid mehr und qualitativ besseres Blau ergibt. Spuren der Blaufärberei lassen sich in Indien und China bis ins 3. Jahrtausend v. Chr. nachweisen. Auch die Aegypter kannten die Kunst des Färbens mit Indigo. In Grabkammern fand man Mumien, die in blaugefärbte Bänder eingewickelt waren. Indigo wurde schon im 1. Jahrhundert v. Chr. in der Medizin als Adstringens (zusammenziehendes Mittel) bei Entzündungen und Geschwülsten, aber auch zur Reinigung und Heilung von Wunden verwendet. Bedingt durch den eingeschränkten Handel mit dem Orient war in der Antike und im Mittelalter der Indigo in Europa fast unbekannt und wurde aufgrund des hohen Preises nur als Malerfarbe verwendet.
Die ersten sicheren Angaben über die orientalische Färbekunst von Textilien brachte um 1300 der Venezianer Marco Polo (1254-1324) von seinen Reisen mit. Er beschreibt in seinen Reiseberichten die Gewinnung von Indigo im Königtum Kulam an der Westküste Indiens und erwähnt Gujarat und Cambai in Nordwestindien als Zentren der Indigofabrikation. Weitere Hauptanbaugebiete befanden sich auf den Sundainseln, besonders auf Java. Diese Pflanze wurde dann jahrhundertelang in Indien, Indonesien und viel später durch die europäische Kolonisation auch auf den Antillen und in Amerika in grossen Mengen landwirtschaftlich angebaut.

Abbildung 3: Indigofera tinctoria
Die abgeschnittenen Pflanzen wurden zusammen mit Wasser und verschiedenen Zugaben bei einer Temperatur von 35°C vergoren. Nach etwa 18 Stunden wurde die Flüssigkeit in ein tiefergelegenes Becken abgelassen, wo sie mit Ruten oder Holzlatten während einiger Stunden geschlagen wurde (Abb. 4). Der Sauerstoff, der durch diese Behandlung in die Lösung gelangt, oxidiert das lösliche Indoxyl zu Indigo. Gleichzeitig treibt er störendes Kohlendioxid, das sich bei der Gärung gebildet hat, aus. Der wasserunlösliche Farbstoff scheidet sich allmählich in Form von blauen Flocken ab. Diese Flocken wurden gesammelt, getrocknet und in Stücke gepresst.

Abbildung 4: Indigogewinnung auf Java
2.3 Gemeinsamkeit - das Blau
Chemisch gesehen interessant an diesen beiden Pflanzen ist, dass der blaue Farbstoff in einem farblosen Vorprodukt vorkommt, das wir heute Indoxyl nennen:
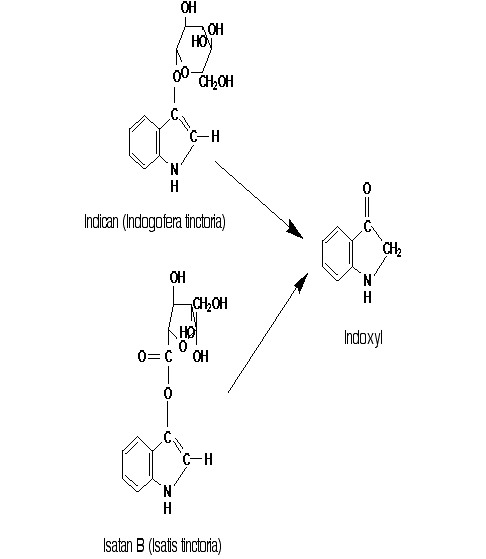
Abbildung 5: Gemeinsames Blau.
An dieses Indoxyl ist, je nach Pflanze, ein Zuckermolekül chemisch gebunden (Abb. 5). Durch einen Fermentationsprozess muss diese Bindung zunächst gelöst werden. Beim Waid wurde das zerstossene Pflanzenmaterial unter Zugabe von Urin vergoren. Dieser Prozess wurde in Kübeln durchgeführt; entsprechend nannte man die entstandene Brühe Küpe. Daraus leitet sich der auch heute noch gebräuchliche Begriff ¨Küpenfarbstoff¨ ab.
Tränkt man nun Textilmaterial mit dieser farblosen Brühe und legt es dann an die Sonne, so erscheint die blaue Farbe (Abb. 6).
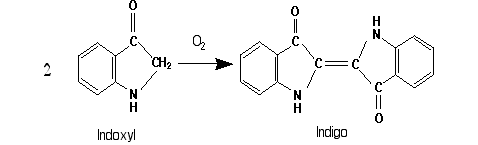
Abbildung 6: Vom Indoxyl zum Indigo.
Natürlich wussten die damaligen Färber nichts von Reduktions- und Oxidationsvorgängen. Die Arbeitsvorschriften waren ein streng gehütetes Geheimnis der Färberzünfte und legten den Arbeitsablauf genau fest. Auch blieb die chemische Identität der beiden blauen Naturstoffe lange Zeit unbekannt.
Beide natürlich vorkommenden Indigo waren mit Indigotin, dem cis-Isomeren, und Indirubin (Indigorot) verunreinigt. Die Zusammensetzung variierte stark und verlangte von den Färbern viel Erfahrung beim Umgang mit diesen Stoffen.
2.4 Untergang des Färberwaid
Nach der Entdeckung des Seeweges nach Indien im Jahre 1498 durch Vasco da Gama fand der asiatische Indigo durch portugiesische Handelsleute schnell Zugang nach Europa. Die Portugiesen nannten den neuen Handelsstoff Anil, nach dem altindischen Wort “nilah“, was schwarzblau bedeutet.
Anfänglich bereitete der Umgang mit diesem neuen Indigo grosse Schwierigkeiten. Zur Ueberführung in die zum Färben geeignete Leukoform (so nennt man die reduzierte Form des Farbstoffes) verwendete man zunächst Operment (Arsensulfid); eine Methode, die vermutlich von den indischen Färbern übernommen wurde. Operment - auch Rauschgelb genannt - war aus der Schwarzfärberei bekannt, da Arsensulfid mit Eisen einen schwarzen Niederschlag bildet. Das Arbeiten war für den Färber mit grossen gesundheitlichen Risiken verbunden und die ätzende Wirkung des Operment auf die Faser trug dem Indigo bald den Ruf als "Corrosivfarbe" ein. Später verwendete man eine Vitriolküpe aus Eisensulfat und Kalk zur Reduktion des Indigos. Eisenvitriol machte aber die Fasern hart und brüchig und führte zu einer Schädigung des Gewebes. Aus diesen Gründen - und wohl auch zum Schutz der Waidbauern - wurde diese "fressende Teufelsfarbe" in einer kaiserlichen Reichspolizeiverordnung 1577 verboten und das Färben sowie das Anbieten von gefärbten Stoffen unter Strafe gestellt. Frankreich ging schon 1558 einen Schritt weiter und untersagte die Indigofärberei bei Androhung der Todesstrafe. Einzig in England, wo nur wenig Waid angebaut wurde, stiess der Indigo auf keine Abwehr.
Trotzdem wurde mit Indigo weiterexperimentiert. Häufig verwendeten die Blaufärber eine Waidküpe, indem sie beim für Waid üblichen Verfahren blieben und einfach die grösste Menge des Waides durch asiatischen Indigo ersetzten. Bald kamen neue, einfachere Gärungsküpen hinzu (etwa die Pottasche- und Sodaküpe) und die alte Urinküpe spielte nur noch eine untergeordnete Rolle. Die Urinküpe ist nur schwach alkalisch und eignete sich besonders für das Färben von Wolle, da diese besonders empfindlich auf hohe pH-Werte reagiert. Besonders in der bäuerlichen Hausfärberei blieb die Urinküpe bis in unser Jahrhundert erhalten.
Je besser man den Umgang mit dem asiatischen Indigo beherrschte, um so mehr trat der Waid in den Hintergrund. Die Portugiesen wurden in Indien durch die Holländer verdrängt und mit der Gründung der Ostindischen Handelsgesellschaft im Jahre 1602 wurde die Indigoeinfuhr aus Indien und Indonesien nach Europa intensiviert. Die Spanier führten dann die Indigopflanze auch in den von ihnen besetzten Gebieten in Mittel- und Südamerika ein und es entstanden dort grosse Indigoplantagen. Und damit begann auch das Leiden und Sterben tausender von Sklaven, die von Afrika aus in die neu angelegten Plantagen gebracht wurden. Frankreich förderte den Anbau auf San Domingo, ihrer wichtigsten Besitzung in Westindien, und die Engländer gründeten um 1700 die ersten Indigoplantagen in Karolina.
Der Untergang des in Europa noch in hoher Blüte stehenden Färberwaid-Indigos war damit trotz grossem Widerstand der Waidbauern besiegelt (damals gab es noch keine EG mit ihrer Agrarordnung). Insbesondere der Ausbruch des 30jährigen Krieges im Jahre 1618 führte zu einer Verknappung des Waides, da viele Waidacker nicht mehr richtig bestellt werden konnten oder zur Gewinnung von Nahrungsmitteln genutzt wurden. In diese Lücke trat nun der weitaus billigere und qualitativ bessere asiatische Indigo.
Nach dem Verlust der nordamerikanischen Kolonien (1783) intensivierte England den Indigoanbau in Bengalen. Nach dem Aufstand der Mulatten und Neger in San Domingo (1795) eroberte sich Grossbritannien eine Monopolstellung im Indigohandel. Darauf versuchte Napoleon I durch Förderung des Waidanbaus und mit einer Importsperre englischer Produkte zu antworten. Er setzte 1810 einen Preis von 425 000 Franken für die Verbesserung der Waidfärberei oder das Auffinden einer leicht anbaubaren Ersatzpflanze aus. Ein Jahr später wurde der Waidanbau in ganz Frankreich gesetzlich angeordnet. Doch alle diese Bemühungen führten infolge der nur noch kurzen Lebensdauer des Kaiserreiches zu keinem Erfolg.
Im Laufe des 19. Jahrhunderts erlebte die Indigoproduktion dank dem intensiven Anbau in Britisch-Indien eine beträchtliche Steigerung. Rund 75 % der Weltproduktion stammten aus diesem Gebiet. Java und Ceylon, Guatemala, San Salvador, Nicaragua, Mexico und Venezuela waren weitere wichtige Exportländer. Wie alle Monokulturen waren auch die grossen Indigoplantagen anfällig für Schädlinge und nicht selten wurde die ganze Ernte vernichtet.
In ganz Europa wurde nun mit diesem natürlichen Farbstoff aus fernen Ländern Blaufärberei betrieben. Auch in unserer Sprache hat sie Spuren hinterlassen. Nach zwölfstündigem arbeitsintensiven Ansetzen der Küpe und der Behandlung des textilen Materials in der Küpe folgte das ebenso lange Hängen an der Luft. Sonntags wurde nicht gearbeitet; so lag das Färbegut einen Tag mehr in der Küpe. Am Montag wurde dann “Blau gemacht“. Man begann die neue Arbeitswoche also eher gemächlich und wir kennen heute noch die Bezeichnung vom “blauen Montag“.
1897 betrug die Weltproduktion von natürlichem Indigo neun Millionen Kilogramm. In Indien umfasste die Anbaufläche für Indigo rund 650 000 Hektaren. Kalkutta wurde zum wichtigsten Handelsplatz für Indigo.
Die reinsten Sorten des natürlichen Indigos enthielten bis 90% Farbstoff und stammten vorwiegend aus Java. Bei schlechteren Sorten betrug der Farbstoffgehalt 20% oder weniger. Es ist klar, dass versucht wurde, dieses kostbare Handelsprodukt durch Zugabe von Stärke, Berlinerblau, Russ, Harz und zerkleinerten, blauen Woll- und Seidenstoffabfällen zu strecken.
Einen weiteren Aufschwung erlebte die Indigofärberei 1873. Der französische Chemiker Paul Schützenberger* (1829-1897) entdeckte die hydroschweflige Säure und das als starkes Reduktionsmittel wirkende Natriumhydrosulfit. Damit begann eine neue Epoche in der Geschichte der Küpenfärberei. Erstmals war es möglich, die Indigoküpe in einfacher und sicherer Form anzusetzen, besonders später mit dem, einen konstanten Farbstoffgehalt aufweisenden, synthetischen Indigo. In kurzer Zeit (kalt in 60 Minuten, bei Erwärmen in 30 Minuten) war die Reduktion vollzogen.
An dieser Stelle eine kurze Nebenbemerkung. Im Auftrage eines Amsterdamer Handelsgeschäftes war ein tüchtiger Kaufmann in Russland im Indigogeschäft tätig. Dieser brachte es dank der grossen Nachfrage schnell zu Reichtum und konnte es sich leisten, sich ganz seiner Leidenschaft, der Archäologie, zuzuwenden. So stehen die Ausgrabungen von Heinrich Schliemann in Troja (1870) und Mykene in einem nachweisbaren Zusammenhang mit dem Indigo.
Während der Indigo immer noch Höchstpreise erzielte, war sein Schicksal schon besiegelt. Mit der Gründung der Teerfarbenindustrie begann eine Umwälzung, die die Färberei völlig umgestalten und die Herrschaft der synthetischen Farbstoffe begründen sollte.
3. Strukturaufklärung und Synthese
Allmählich begann sich die wissenschaftliche Chemie mit dem Indigo zu befassen. Die einfachste Reinigungsoperation für eine Substanz bestand darin, sie zu verdampfen und wieder zu kondensieren. 1826 versuchte der Apotheker Otto Unverdorben* dieses Verfahren mit Indigo. Die Substanz zersetzte sich dabei und Unverdorben nannte das flüssige Zersetzungsprodukt in Anlehnung an die portugiesische Sprache Anilin.
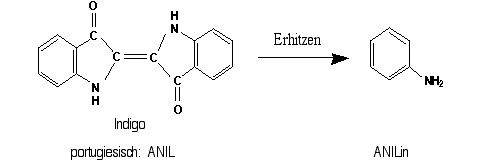
Abbildung 7: Abbau zum Anilin.
Damit war der Weg für einen neuen, wichtigen Industriezweig vorgezeichnet. Manche Firmen tragen heute noch das Anilin im Firmennamen, so z.B. die Badische Anilin und Sodafabrik (BASF) oder die Aktiengesellschaft für Anilinfarben (AGFA).
1841 wurde durch Abbau unter milderen Bedingungen aus dem Indigo die Anthranilsäure gewonnen. Weitere Abbaumethoden führten später zum Indol und zum Isatin. Die Namen dieser Substanzen verraten den ursprünglichen Zusammenhang mit den natürlichen Farbprodukten (Abb. 8). Nun erst wurden auch die chemischen Zusammenhänge zwischen dem Färberwaid und dem asiatischen Indigo erkannt.

Abbildung 8: Abbau zu Indol und Isatin.
1865 beginnt Adolf von Baeyer* mit der Strukturaufklärung und Synthese des Indigos. Seine ersten Erfahrungen mit Indigo machte Baeyer schon mit 13 Jahren, als er mit seinem Taschengeld ein Stück davon kaufte und nach dem Chemiebuch von Wöhler weiterverarbeitete.
Bis zum Abschluss dieser Arbeiten sollten 15 Jahre vergehen. Einen ersten Erfolg erzielte Baeyer schon 1866, als es ihm durch Zinkstaubdestillation gelang aus dem Indigo Indol herzustellen. 1870 stellte er den ersten synthetischen Indigo durch Chlorierung und anschliessende Reduktion von Isatin her. Da aber das Isatin durch Oxidation von Indigo erhalten wurde, stellte sich nun das Problem nach einer machbaren Isatinsynthese. Es brauchte weitere 8 Jahre bis die Herstellung von Isatin aus Phenylessigsäure glückte und die erste wirkliche Vollsynthese von Indigo erfolgte am 6. Juni 1878. Doch die genaue Struktur von Indigo blieb immer noch unbekannt. Bei seinen Arbeiten wurde Adolf von Baeyer stark vom damaligen technischen Direktor der BASF, Heinrich Caro, unterstützt. Es entwickelte sich für Jahre eine gute Zusammenarbeit zwischen Hochschule und Farbstoffindustrie. Es folgte eine Zahl von weiteren Synthesen für Indigo, die allerdings wegen den kleinen Ausbeuten und den Kosten für die Edukte technisch nicht machbar waren.
Im Jahre 1880 glückte Baeyer eine neue Herstellungsmethode aus Zimtsäure (Abb. 10). Es zeigte sich bald, dass zur Herstellung von Indigo, Isatin und Indol die Zimtsäure ein besseres Ausgangsmaterial war alle bisher verwendeten. Am 19. März 1880 wurde die erste Indigosynthese ausgehend von o-Nitrozimtsäure patentiert (Deutsche Patentschrift 11 857)
Abbildung 9: Adolf von Baeyer
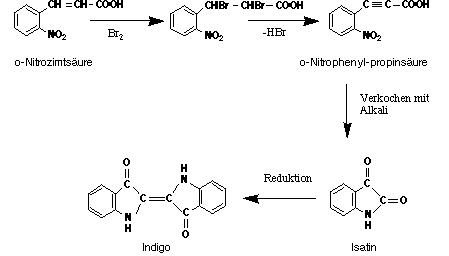
Abbildung 10: Erste Indigosynthese nach Adolf von Baeyer.
Ein weiteres von Baeyer im Jahre 1883 patentiertes Verfahren geht von o-Nitrobenzaldehyd aus (Abb. 11). Mit Hilfe dieser Synthese konnte nun erstmals die Struktur von Indigo eindeutig festgelegt werden. Baeyer konnte befriedigt bemerken, dass nun jedes Atom im Molekül seinen Platz gefunden hat. Die genaue Struktur - nämlich die trans-Form - konnte erst nach dem Tod von A. von Baeyer durch Röntgenstrukturanalyse im Jahr 1928 einwandfrei festgestellt werden. Mit 4-Brom-2-nitrobenzaldehyd als Edukt konnte später mit dieser Methode das 6,6'-Dibromindigo (Purpur) dargestellt werden.
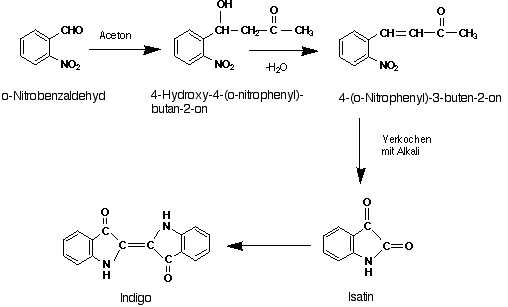
Abbildung 11: Zweite Indigosynthese nach Adolf von Baeyer.
Für den Universitätsprofessor A. von Baeyer war damit die Arbeit mit Indigo abgeschlossen. Die weitere Nutzung und Anwendung seiner Forschung war ihm gleichgültig. Dies ist ein gutes Beispiel für den Unterschied zwischen rein akademischer und industrieller Forschung.
Die von Baeyer gefundenen Synthesen erwiesen sich als unwirtschaftlich, da durch rationellen Plantagenanbau der indische Indigo zu einem Preis auf den Markt kam, der für die Herstellung des synthetischen Produktes enge Grenzen setzte. Insbesondere die aromatische Nitrierung bereitete Schwierigkeiten, da sie immer zu einem Isomerengemisch führte. Doch war es Adolf von Baeyer, der grundsätzlich zeigte, dass die Synthese von Indigo möglich ist. Ein Meilenstein in der Entwicklung der synthetischen Farben war gelegt.
Doch muss an dieser Stelle auch auf die Kehrseite der Entwicklung hingewiesen werden. Flüsse wurden als Abwasserkanäle missbraucht und mit Gift- und Reststoffen aller Art belastet. Viele der neuen Farben erwiesen sich zudem als giftig und die gesundheitsgefährdenden Arbeitsbedingungen in den neuen Fabriken prägten bald die Begriffe “Anilinhölle” und “Giftküche”.
Nun setzte eine stürmische Entwicklung ein und viele neue Verfahren zur Herstellung von Indigo wurden patentiert (unter anderem auch in Basel bei Geigy mit der von Traugott Sandmeyer* entwickelten Thiocarbanilid-Synthese)
Besonders wichtig war eine von Karl Heumann* (1851-1894) am 6. Mai 1890 patentierte, von Anilin ausgehende Synthese. Heumann fand in der Alkalischmelze von N-Phenylglycin 10% Indigo. Alle für die technische Synthese von Phenylglycin gebrauchten Edukte wie Anilin, Essigsäure, Chlor und Alkali standen schon damals in ausreichender Menge billig zur Verfügung (Abb. 12).
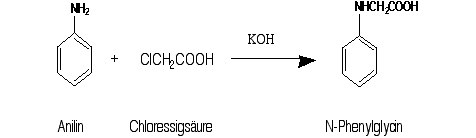
Abbildung 12: N-Phenylglycin aus Anilin.
Noch im gleichen Jahr entwickelte Heumann eine zweite, von Naphthalin ausgehende Sythesefolge (Abb. 13). Endprodukt war die N-Phenylglycin-o-carbonsäure, die in der Alkalischmelze wesentlich grössere Ausbeuten (bis 90%) an Indigo liefert.

Abbildung 13: N-Phenylglycin-o-carbonsäure aus Naphthalin.
Der gebürtige Darmstädter Heumann war zu dieser Zeit Professor an der ETH in Zürich. Die Schweizer Industrie verpasste die einmalige Gelegenheit und so wurden seine Erfindungen von der BASF und von der Firma Meister, Lucius & Brüning (später wurde daraus die Hoechst AG) patentiert und weiterentwickelt. Den wirtschaftlichen Durchbruch seines Verfahrens durfte Heumann nicht mehr erleben.
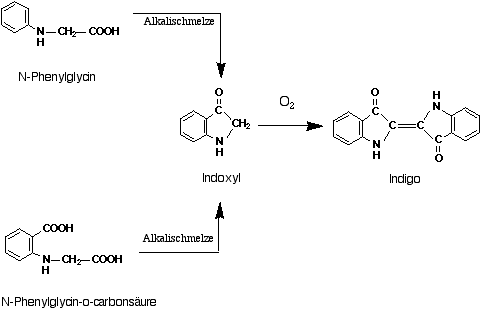
Abbildung 14: Indigosynthesen nach Heumann.
Doch mussten nochmals sieben Jahre vergehen, bis der erste synthetische Indigo durch die BASF auf den Markt kam. In dieser Zeit wurden viele technische Verfahren zur Gewinnung der Grundsubstanzen (z.B. das wichtige Schwefelsäure-Kontakt-Verfahren) entwickelt.
4. Andere Blaufarbstoffe, das erste Medikament von Bayer
Die Farbenfabriken waren in der Zwischenzeit nicht untätig und versuchten ihr Geschäft mit anderen Blaufarben. 1886 brachte Bayer mit grossem Werbeaufwand den Azofarbstoff Benzazurin G (Abb. 16) heraus, der besser als Indigo sein sollte. Man plante bei Bayer schon den Bau einer neuen Fabrik, die 10 000 Kilogramm täglich produzieren sollte. Die Versprechungen waren zu hoch gegriffen, denn an der Sonne trat schon nach Stunden eine rötliche Verfärbung auf. Doch in Ermangelung eines besseren Farbstoffes kletterte die Tagesproduktion bald auf über 1000 Kilogramm. In einem ersten Schritt wurde Phenol nitriert (Abb. 15).
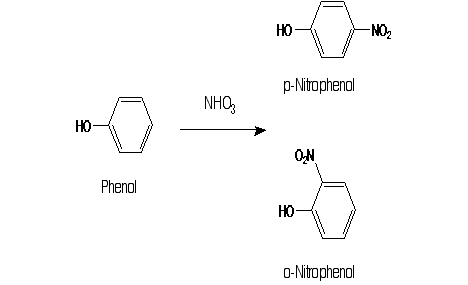
Abbildung 15: Nitrierung von Phenol
Als Nebenprodukt fielen grosse Mengen p-Nitrophenol an, das zu dieser Zeit nicht weiterverwendet wurde und in Fässern abgefüllt auf dem Werksgelände lagerte. Bald war die ganze Fabrik mit diesen Fässern überstellt - eines der ersten grossen Entsorgungsprobleme der jungen technischen Chemie.
Nach Methylierung der OH-Gruppe und Reduktion der Nitrogruppe zum Amin entstand o-Methoxyanilin (o-Anisidin), aus dem sich durch eine Benzidin-Umlagerung leicht das entsprechende Dianisidin herstellen lässt. Durch Diazotieren und Kuppeln auf 1-Naphthol-4-sulfonsäure lässt sich der Farbstoff gewinnen.
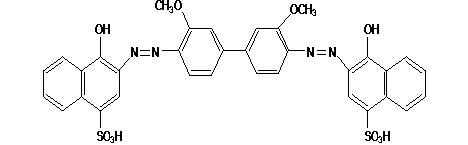
Abbildung 16: Benzazurin G
Bei der Lösung des Abfallproblems war wie so oft in der Geschichte auch hier der Zufall im Spiel. Ein Strassburger Apotheker verkaufte zwei jungen Aerzten (Dr. Kahn und Dr. Hepp) Acetanilid anstelle von Naphthalin. Die beiden Mediziner wollten die von ihnen vermutete fiebersenkende Wirkung von Naphthalin an einem an Staupe erkrankten Hund ausprobieren und fanden so die unerwartete Eigenschaft von Acetanilid. Kalle & Co. in Biberich brachte Acetanilid unter dem Namen Antifebrin auf den Markt. Doch war das erste synthetische Medikament nicht frei von unangenehmen Nebenwirkungen. Den Bayer-Werken gelang daraufhin die Gewinnung eines im Vergleich zu Acetanilid weniger giftigen Stoffes aus dem störenden p-Nitrophenol und sie brachten 1888 mit dem Phenacetin (Abb. 17) ihr erstes erfolgreiches Medikament heraus und machten den ersten Schritt weg von einer reinen Teerfarbenfabrik.
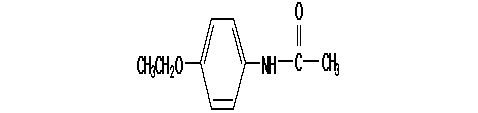
Abbildung 17: Phenacetin, N-(4-Ethoxyphenyl)-acetamid.
Das Medikament kam gerade rechtzeitig, denn 1889 ging eine Influenza-Welle durch die Welt, von der vor allem Amerika stark betroffen war. Phenacetin wurde zur Hilfe für unzählige Kranke.
Phenacetin wirkt bei Migräne, Ischias, Neuralgien, Rheuma usw. und war bis zum Verbot 1986 in zahlreichen schmerzstillenden und fiebersenkenden Präparaten enthalten. Der Dauerkonsum führt zu Nierenschädigung und erhöhtem Krebsrisiko.
Die Suche nach einem blauen Farbstoff führte also indirekt auch zu der Entwicklung der Pharmaindustrie, denn viele Farbenfabriken begannen nun mit der Produktion von Arzneimitteln.
5. Synthetischer Indigo
Doch zurück zum König der Farbstoffe. Beim ersten der beiden Heumann-Synthesen bot der Ausgangsstoff keine Schwierigkeiten. Phenylglycin lässt sich leicht aus Anilin und Chloressigsäure darstellen. Doch die Weiterverarbeitung zum Farbstoff führte in eine Sackgasse; die Ausbeute war einfach zu gering und das Verfahren unrentabel.
Bei der Methode über die N-Phenylglycin-o-carbonsäure war technisch schon der erste Schritt, die Oxidation von Naphthalin zu Phthalsäureanhydrid, problematisch. Dieser Reaktionsschritt konnte zunächst nur mit der teuren Salpetersäure durchgeführt werden, und das machte das Verfahren zu kostspielig. Und hier trennen sich die Wege von BASF und Hoechst auf der Suche nach einem billigen Oxidationsmittel.
Hoechst versuchte es zunächst mit Chromsäure und Chromaten. Dieser Weg war zwar machbar, doch brachte wirtschaftlich keinen Erfolg, solange es nicht möglich war, die Chromlaugen billig wieder in Chromsäuren zurückzuführen. Mit Hilfe der Elektrochemie fand man die Lösung, doch es fehlte vorerst die Versorgung mit billigem Strom. Mit einer Elektrizitätsgesellschaft schloss man einen Vertrag zur Gewinnung von Strom aus dem Lech und kaufte bei Augsburg ein Baugelände. Auf diesem wurde ein Werk errichtet, das Indigo und seine Vorprodukte produzieren sollte.
Während bei Hoechst die neue elektrochemische Anlage entstand, arbeitete die BASF an der Oxidation von Naphthalin mit rauchender Schwefelsäure. Die ersten Resultate waren alles andere als vielversprechend. Da kam ein Zufall - einer der berühmtesten in der Chemiegeschichte - ins Spiel. Bei einem Versuch zerbrach das Thermometer und Quecksilber floss in den Reaktionskolben. Die bekümmerten Gesichter der Chemiker hellten sich schnell wieder auf, als sich zeigte, dass Quecksilber der ideale Katalysator für diese Oxidation war. Die BASF war nun am Ziel ihrer Wünsche: jahrelanges Forschen und Investitionen von 18 Millionen Mark (dem ganzen Aktienkapital) waren nicht vergebens. Im Februar 1897 begann die Produktion und im Juli war der erste synthetische Indigo auf dem Markt.

Abbildung 18 : Indigo-Etikette
Anfänglich begegnete man in Färberkreisen dem neuen Produkt mit grossen Vorurteilen und Zurückhaltung. Zudem erwuchs der BASF bald ernsthafte Konkurrenz, denn 1901 stellte Johannes Pfleger* (1867-1957) bei der Degussa (Deutsche Gold- und Silberscheidanstalt) fest, dass N-Phenylglycin sich in der Alkalischmelze unter Zusatz von Natriumamid in 90%iger Ausbeute in Indigo umwandeln lässt. Natriumamid fiel bei der Degussa als Nebenprodukt bei der Gewinnung von Natriumcyanid an, das zur Extraktion von Edelmetallen benötigt wird. Die Wirkung von Natriumamid beruht vermutlich darauf, das auch die letzten Spuren von Wasser gebunden werden. Die Temperatur der Ringschlussreaktion konnte von 300°C auf 200°C gesenkt werden. Die thermische Zersetzung des gebildeten Indoxyls wird so weitgehend verhindert.
Das Verfahren wurde von den Farbwerken Hoechst (vormals Meister, Lucius und Brüning) übernommen und als Indigo ML&B in den Handel gebracht. Die BASF verlor ihre Vormachtstellung und ein heftiger Konkurrenzkampf begann. Schliesslich wurde der Markt 1904, nachdem der Preis auf 7 Mark pro Kilogramm gesunken war, durch den Abschluss einer Konvention aufgeteilt. Der Ausbau des elektrochemischen Werkes in Augsburg wurde nicht fortgeführt, denn das Pfleger-Verfahren verdrängte bald alle anderen. Im Jahre 1913 produzierte alleine Hoechst 4,5 Millionen Kilogramm Indigo. 1926 schlossen die beiden deutschen Werke einen Vertrag, der es allen erlaubte, nach der kombinierten Heumann-Pfleger-Methode zu produzieren. Dieser Vertrag bildete eine Vorstufe zur Gründung der IG-Farben.
1900 musste Deutschland noch für 20 Millionen Mark Naturindigo importieren, doch schon 1905 erreichte der Export von synthetischem Indigo einen Wert von 25 Millionen Mark.
Das stolze Englische Indigo-Monopol geriet so erst ins wanken und zerbrach dann in kurzer Zeit ganz (und ein weiterer Schritt zum Untergang der einstigen Weltmacht war gemacht). Das deutsche Nationalbewusstsein bekam dadurch deutlichen Auftrieb. Zum ersten Mal war es durch moderne Technik und Wissenschaft gelungen, einer grossen Kolonialmacht eine Monopolstellung zu entreissen.
Der natürliche Indigo erlebte während dem ersten Weltkrieg eine neue kurze Blüteperiode, weil zahlreiche Staaten vom Bezug des nur in Deutschland und in der Schweiz hergestellten synthetischen Indigos abgeschnitten waren. Nach der Wiederaufnahme der Fabrikation, nun auch in anderen Ländern, sank der Verbrauch des Naturstoffes sehr schnell. 1930 war dann die Indigokultur in Britisch-Indien so gut wie erloschen.
Heute wird Indigo immer noch aus Phenylglycin hergestellt, das durch Verseifen von Phenylaminoacetonitril gewonnen wird (Abb. 19).
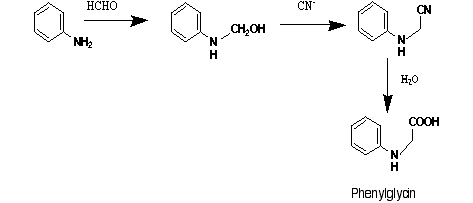
Abbildung 19: Heutige Methode zur Herstellung von Phenylglycin.
Neben dem Indigo wurden viele weitere indigoide Farbstoffe hergestellt, die einige Zeit besonders im Textildruck eine wichtige Rolle gespielt haben. Wichtig war der von Paul Friedländer 1905 entwickelte Thioindigo, bei dem die NH-Gruppe des Indigo durch Schwefel ersetzt ist. Dieser Farbstoff wurde von Kalle-Biebrich unter dem Namen Thioindigorot fabriziert und erfreute sich damals grosser Beliebtheit.
6. Indigo in unserem Jahrhundert
Was lange Zeit heiss ersehnt und mit grossem Einsatz gesucht wurde, stand nun mehrfach zur Verfügung: Wege zum synthetischen Indigo. Doch die Vormachtstellung sollte nicht lange halten, denn nun waren auch erstmals die chemischen Vorgänge der Küpenfärberei klar und es dauerte nicht lange, bis auch andere Farbstoffe (vor allem Anthrachinonfarbstoffe) durch Reduktion in lösliche Form gebracht und so auf die Faser appliziert wurden. Durch Oxidation konnte man eine dauerhafte Fixierung auf der Faser erreichen. Und auf einmal wurde man auf eine Unzulänglichkeit von Indigo aufmerksam: Diese neuen Farbstoffe hatten bessere Wasch- und Reibeigenschaften als der König der Farbstoffe.
So gelang schon 1901 René Bohn* (1862-1922) in der BASF die Indanthren-Synthese durch Verschmelzen von 2-Amino-anthrachinon in Alkali (Abb. 20)
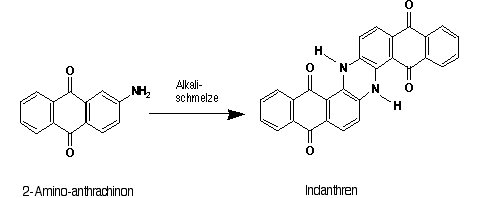
Abbildung 20: Indanthren-Synthese.
Der von Bohn ursprünglich verwendete Namen Indanthren zeigt seine eigentliche Absicht auf: Indigo aus Anthrachinon. Das gelang zwar nicht, doch das erhaltene Produkt war ebenfalls blau.
R. Bohn schreibt über diesen neuen Farbstoff: "Dieses neue Blau lässt sich wie Indigo ausfärben und hat die gleiche Lichtechtheit. Aber der Farbstoff sitzt auf der Faser wie eingebrannt".
Dieser Farbstoff wurde 1903 von der BASF als Indanthrenblau RS und 1906 von Bayer unter dem Namen Algol mit einem für die damalige Zeit grossen Werbeaufwand eingeführt. Eine völlig neue Marktstrategie wurde dafür entwickelt. Nicht mehr nur der Färber alleine sollte von der Qualität der Produkte überzeugt werden, sondern vielmehr der Verbraucher. Der Konsument soll von nun an dem Markt befehlen, was dieser zu produzieren hat.
Das neue Syntheseprinzip beschränkte sich nicht nur auf Blau. Bald folgten weitere Farbstoffe mit ähnlich hoher Echtheit und der Begriff Indanthren wurde 1922 zum Markenzeichen für alle hochwertige Küpenfarbstoffe (Abb. 21).

Abbildung 21: Indanthren Markenzeichen
Und schon bald kamen billige blaue Schwefelfarbstoff auf den Markt und traten in Konkurrenz zum Indigo.
Zunächst aber konnte der Indigo jedoch seine Vormachtstellung behalten. Manche Färber blieben aus Tradition bei ihrem Farbstoff. Doch wurde der charakteristische Geruch vermisst, und so mussten dem Industrieprodukt zunächst noch Stinkstoffe zugesetzt werden. Durch immer grössere und verbesserte Produktion sank der Preis für Indigo kontinuierlich. Dem Indigo kam zugute, dass der Markt für blaue Arbeitskleidung mit zunehmender Industrialisierung stark zunahm. Ein grosser Teil des Exportes ging dann nach China für die blauen Kittel der fleissigen Mao-Ameisen. Bald verbrauchte China mehr Indigo als alle anderen Länder zusammen. Das königliche Blau des Altertums und des Mittelalters wurde so zum Farbstoff der breiten und gewöhnlichen Masse.
Trotzdem ging der Bedarf an Indigo immer mehr zurück und viele Firmen stellten die Produktion ein. Lange Zeit wurde Indigo nur noch zur Herstellung von Isatin, einem wichtigen Zwischenprodukt für andere Farbstoffsynthesen, verwendet. Als dann auch für Isatin ein neuer Herstellungsweg gefunden wurde, spielten viele Hersteller mit dem Gedanken, die Produktion ganz einzustellen. Doch rechtzeitig begann eine neue Aera in der wechselvollen Geschichte des Indigos.
7. Indigo - Jeansblau
Blenden wir einige Zeit zurück. Im Jahre 1850 wandert ein zwanzigjähriger Kaufmann namens Levi Strauss (26.2.1829-26.10.1902) aus Buttenheim (Oberfranken) nach San Francisco aus. Zu dieser Zeit herrschte im Westen der USA der Goldrausch und Levi Strauss stellte aus indigogefärbtem Drillich strapazierfähige Arbeitskleider her. Den Drillich führte er aus dem französischen Nîmes ein. Aus dem "Bleu de Nîmes" wurde so das amerikanisierte "Blue Denim", die heute noch übliche Bezeichnung für diese Textilart. Den benötigten Indigo importierte man über Genua in die USA. Aus "Bleu de Gênes" wird da "Blue Jeans". 1872 wurden die bekannten Kupfernieten zur Verstärkung eingeführt und patentiert.
Und die neue Jeanswelle am Ende der sechziger Jahre verhalf dem Indigo zu einem Comeback. Der Jugend war alles Perfekte suspekt und so wurden die mit Indigo, einem nicht ganz so perfekten Farbstoff, gefärbten Jeans zum Ausdruck einer veränderten Lebenseinstellung. Aus dem König der Farbstoffe wurde ein Symbol der Nonkonformisten. Heute sind die Jeans schlicht und einfach legere Freizeitmode - alle tragen Jeans.
Die Jahresproduktion von Indigo betrug 1988 wieder stolze 14'000 Tonnen (Tendenz steigend), die zu 90% zum Färben von Jeanskleidung verwendet werden. Für ein Paar Jeans werden, je nach Qualität, 3 bis 12 g Indigo benötigt. Das entspricht bei einem Indigopreis von 30 Franken pro Kilogramm einem Wert von 10 bis 35 Rappen. Obwohl die Weltproduktion in der Grössenordnung von einer Milliarde Indigo-Jeans pro Jahr liegt, spielt Indigo mit einem Weltjahresumsatz von gut 400 Millionen Franken für die Chemieindustrie wirtschaftlich nur noch eine untergeordnete Rolle. Die Buffalo Color Corp. in den USA, die BASF in Deutschland, ICI (Imperial Chemicals Industries) in England und Mitsui Toatsu in Japan sind heute die vier führenden Gesellschaften zur Herstellung des synthetischen Indigos.
Ueber 400 Produzenten stellen heute Jeans her und färben sie mit Indigo. Mehr als 70% der Textilien stammen aus dem fernen Osten, insbesondere aus Hong Kong. Asien ist auch der grösste Absatzmarkt für Jeans, gefolgt von den USA und Europa.
8. Ein Indigoverwandter - der Purpur
Um 1500 v.Chr. fanden die Phönizier, dass bestimmte fleischfressende Meeresschnecken (Murex brandaris und Murex trunculus) an der Wand ihrer Atemhöhle einen farblosen Schleim absondern, der auf textilen Fasern an der Luft und mit Licht eine tiefviolette Färbung ergibt.

Abbildung 22: Murex brandaris und Murex trunculus
Eine antike Sage beschreibt diese Entdeckung so: Der Hund des phönizischen Schutzgottes Melkarth zerbiss beim Spiel am Strand eine Schnecke und bekam ein rotes Maul. Melkarth färbte daraufhin für seine Geliebte, die Nymphe Tyros, ein Kleid.
Da eine Schnecke nur sehr wenig Schleim enthielt, war die Gewinnung mühsam und die Färbetechnik aufwendig. Um den Schleim zu erhalten, wurden die Schnecken getötet, zerstampft und mit Salz versetzt. Nach drei Tagen wurde mit Wasser und Urin verdünnt und zehn Tage lang gekocht. Fleischteile und sonstige Fremdkörper wurden dabei sorgfältig abgeschöpft. Dieser Vorgang war natürlich mit Geruchsentwicklung verbunden und so soll es in der bedeutenden phönizischen Handelsstadt Tyrus, einem Zentrum der Purpurgewinnung (wird schon in der Bibel zitiert; Ezechiel 27:7 und zweites Buch Chronik 2:7), ganz erbärmlich gestunken haben. Die Färbekunst verbreitete sich an der Küste von ganz Kleinasien. Auf der Suche nach ertragreichen Fangplätzen bereisten die Phönizier das ganze Mittelmeer und drangen sogar in den Atlantik vor. So findet man an der Nordwestküste von Afrika Spuren der phönizischen Purpurgewinnung. Die Produkte blieben aber wegen des hohen Preises der Oberschicht vorbehalten und Purpur wurde die Farbe der Könige. Und im Buch Moses wird Purpur als Priesterfarbe (Tekhelet) beschrieben (Exodus 26:1,31). Auch Alexander der Grosse und Cleopatra frönten dem Purpurluxus. Bei den Römern war der Purpurmantel das Privileg des Herrschers. Caesar beschränkte das Recht zum Purpur auf sich (als Triumphator) und seine höchsten Beamten, die "vestae clavatae" (Gewänder mit Purpurstreifen) tragen durften. Augustus beschränkte dieses Recht auf die Senatoren. Eine Ausnahme war Tiberius, der den Purpur ablegte, um die Römer durch sein Vorbild von ihrer Purpurlleidenschaft abzubringen. setzte dann für das Tragen des kaiserlichen Purpurs sogar die Todesstrafe aus. Nach Neros Selbstmord wurden die Gesetze gelockert, doch das Tragen vollständig mit Purpur gefärbter Gewänder blieb das Vorrecht des Kaisers.
Zur unsicheren Zeit der Kreuzzüge im 12. Jahrhundert wich die Purpurfärberei nach Sizilien aus, wo sie unter den Normannenkönigen zu besonderem Ansehen gelangte. Mit dem Erscheinen der synthetischen Farben starb die Purpurfärberei in kurzer Zeit ganz aus.
Unabhängig von der Purpurfärberei in Kleinasien entwickelte sich auch in Südamerika eine eigenständige Färbereitechnik. Denn auch in zwei pazifischen Schneckenarten findet man den antiken Purpur (Purpura aperta und Purpura lapillus). Die Indios legten die Schnecken auf feuchtes Gewebe und brachten sie durch Beträufeln mit Zitronensaft zur Absonderung des Sekretes. Die Schnecken wurden danach wieder ins Meer gegeben. Das so behandelte Gewebe verfärbte sich an der Sonne in kurzer Zeit.
1909 gewann der an der Technischen Universität Darmstadt tätige Paul Friedländer* (1857-1923) aus 120 000 Schnecken ca. 1,4 Gramm Farbstoff und konnte damit die Struktur bestimmen (Berichte 42,765). Es handelt sich beim Purpur um das 6,6'-Dibromderivat des Indigos (Abb. 23). Es ist sehr erstaunlich, in der Natur eine Bromverbindung zu finden. Zudem sitzen die Bromatome an den Stellen des aromatischen Systems, die den in der Chemie gültigen Substitutionsregeln widersprechen.
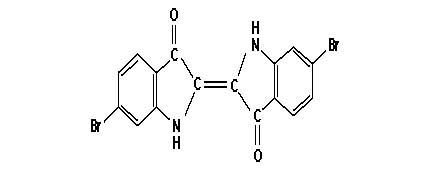
Abbildung 23: 6,6'-Dibromindigo, "Purpur".
Die C=O- Gruppe ist m-dirigierend, die NH- Gruppe o-,p-dirigierend. Daher wird zuerst die 5,5'-Stellung substituiert.
Aus diesem Grund war eine synthetische Herstellung technisch aussichtslos teuer. Während alle anderen Halogenderivate den Farbton des Indigos ins Grünstichige verschieben, ändert sich nur bei der im Purpur vorliegenden Position der Bromatome die Farbe in die rötliche Richtung. Die Sonderstellung, die der Purpur in Geschichte und Kultur eingenommen hat ,ist also auch aus wissenschaftlicher Sicht gerechtfertigt. Sinnlos erscheint mir dagegen der von den Amerikanern in jüngster Zeit gewählte Deckname "Purple" für ein in Vietnam eingesetztes Entlaubungsmittel.
9. Färben mit Indigo:
Indigo gehört in die Gruppe der Küpenfarbstoffe. Für die Küpenfarbstoffe ist charakteristisch, dass sich das Farbstoffmolekül nicht chemisch mit der Textilfaser verbindet. Es haftet als unlösliches Pigment physikalisch auf der Faseroberfläche. Das Hauptanwendungsgebiet der Küpenfärberei ist heute das Färben von Cellulosefasern. Weltweit dürften im Jahr etwa 60'000 Tonnen Küpenfarbstoffe verbraucht werden.
Küpenfarbstoffe sind, wenn man einmal vom Indigo selbst absieht, überwiegend Abkömmlinge des Anthrachinons und Derivate höher kondensierter aromatischer Ringsysteme mit einem geschlossenen System konjugierter Doppelbindungen. Die Zahl der reduzierbaren Carbonylgruppen beträgt in der Regel 2,4 oder 6.
Die Färbung der Textilien mit Küpenfarbstoffen erfolgt aus technischen Gründen meist aus einer wässrigen Lösung, der sogenannten Flotte. Da diese Farbstoffe aber in Wasser unlöslich sind, müssen sie vor der Färbung erst wasserlöslich gemacht werden. Das nennt man Verküpen. Chemisch gesehen ist dies eine Reduktion. Aus dem blauen Indigo entsteht dabei wasserlösliches, hellgelbes “Indigo-Weiss“ bwz. in basischer Lösung sein Natriumsalz (Fig. 24).

Abbildung 24: lösliche und unlösliche Form von Indigo.
Die Farbstoffkonzentration in der Küpe liegt bei 0,15-0,2% Farbstoff.
Das grösste Problem der heutigen Indigofärberei (und der Küpenfärberei) ist der Reduktionsprozess. In den meisten Färbereien verwendet man immer noch Natriumdithionit (Hydrosulfit) als Reduktionsmittel. Daraus entstehen Natriumsulfit und mit dem im Abwasser gelösten Sauerstoff Natriumsulfat. Diese beiden Salze können biologisch nicht abgebaut werden. Unter anaeroben Bedingungen entsteht aus Sulfat giftiger Schwefelwasserstoff. Oft gelangt auch unverbrauchtes Dithionit ins Abwasser. Aus ökologischen Gründen mussten in den vergangenen Jahren mehrere Firmen die Küpenfärberei einstellen oder gar den Betrieb auf behördliche Anordnung hin schliessen.
Das Ueberleben der Küpenfarbstoffe und der Küpenfärberei hängt von der raschen Entwicklung einer neuen biokompatiblen Färbetechnik für diese wichtige Farbstoffklasse ab.
Heute laufen weltweit verschiedene Forschungsprogramme, die einen umweltfreundlicheren Weg für die Küpenfärbung und insbesondere für die Indigofärberei suchen.
Ein Forschungsprojekt der ETH-Zürich verwendet als Reduktionsmittel Hydroxyaceton. Bei einer optimalen Wahl von verschiedenen Prozessparametern gelingt es, einige der wichtigsten Küpenfarbstoffe - wenn auch noch nicht alle - problemlos zu reduzieren. Die Färbung ist bei tiefer Temperatur durchführbar, so dass Energie gespart werden kann. Es hat sich auch gezeigt, dass die Oxidationsprodukte des Hydroxyacetons, und die daraus entstehenden Folgeprodukte, sehr gut biologisch abbaubar sind.
10. Herstellung von Indigo im Labor (J.R. McKee, M. Zanger, J. Chem. Ed. 10, A242, (1991))
Indigo kann nach folgender Vorschrift leicht im Labor hergestellt werden. Die Reaktion verläuft über eine Anzahl von Kondensationen, Disproportionierungen und Oxidationen.
0,5 g o-Nitrobenzaldehyd werden in 5 ml Aceton gelöst und nach der Zugabe von 5 ml Wasser wird gerührt. 2,5 ml einer 1 molaren Natronlaugelösung werden tropfenweise zugegeben. Diese Reaktion verläuft sehr exotherm und die Lösung kann zu kochen beginnen. Nach 5 Minuten wird der ausgefallene Indigo abfiltriert und mit Wasser und Ethanol gewaschen.
Zum Färben wird der gewonnene Indigo in 10 ml Wasser aufgeschlämmt und mit 3 Natronlauge-Plätzchen versetzt. Das Ganze wird aufgekocht und 2 ml einer 10%-igen Natriumdithionitlösung zugegeben. Danach wird noch solange tropfenweise Dithionit zugefügt, bis sich der Indigo klar gelöst hat und in seiner Leukoform vorliegt. Die gelbliche Lösung wird mit 100 ml Wasser verdünnt und kann nun zum Färben von Baumwolle verwendet werden.
*Paul Schützenberger (23.12.1829-16.6.1897)
Machte 1849 unter L. Pasteur in Strassburg das naturwissenschaftliche Bakkalaureat. Er arbeitete als Assistent im Labor von Caillot und ging 1853 als Assistent an das Conservatoire des arts et métiers in Paris. 1854 wurde er Dozent und ein Jahr später Professor an der Gewerbeschule in Mulhouse. Nebenbei setzt er seine medizinische Studien fort und promoviert 1855 als Dr. med. 1863 promoviert er an der Sorbonne als Dr. chem. und wurde Assistent am Collège de France in Paris. 1868 ging er als stellvertrendender Direktor an die Ecole practique des hautes der Sorbonne. 1876 wurde er Professor für mineralogische Chemie am Collège de France und 1882 Direktor der Ecole municipale de physique et de chimie in Paris. Schützenberger lieferte wichtige Beiträge sowohl zur anorganischen wie auch zur organischen Chemie. Es isolierte die farbigen Inhaltsstoffe der Krappwurzel und konnte zeigen, dass nur Alizarin und Purpurin Textilfarbstoffe sind. 1865 stellte er erstmals Cellulosetriacetat her, das Ausgangsprodukt für Acetatseide. 1869 gelang es ihm, die dithionige Säure in Form ihres Natriumsalzes (Natriumdithionit) zu isolieren. Als Indikator verwendete er Indigo, welches durch Dithionit entfärbt (reduziert) wird. Er schlug vor, diese Reaktion bei der Indigo-Verküpung anzuwenden. Bei Arbeiten über Platin, dessen Verbindungen und Legierungen, entdeckt er 1870 die Fähigkeit von CO, NH3 und PCl3 zu recht beständigen Additionsverbindungen. 1875 begann er sich mit Hefe zu befassen. Später dehnte er diese Tätigkeit auch auf Kohlenhydrate aus. Weiter arbeitete er auf dem Gebiet der Metallcarbide und der Isolierung seltener Erden.
*Otto Unverdorben (13.10.1806-28.11.1873)
Ausbildung zum Chemiker in Dresden, Leipzig und Halle. Er untersuchte vor allem die trockene Destillation von organischen Substanzen. Ab 1829 übernahm er eine geerbte Gemischtwarenhandlung und war nicht mehr wissenschaftlich tätig.
*Adolf von Baeyer (31.10.1835-20.8.1917)
Studierte zuerst in Berlin Mathematik und Physik, später in Heidelberg bei Bunsen und Kekulé Chemie. 1858 promovierte er und folgt Kekulé nach Gent. Zurück in Berlin habilitierte er sich 1860 und bekam eine Lehrstelle am Berliner Gewerbeinstitut. Seine Schüler Graebe und Liebermann klärten hier mit der Baeyerschen-Zinkstaubdestillation die Struktur des Alizarins auf und stellten es aus Anthracen her. Nach einem Abstecher an die Universität Strassburg wurde er 1873 als Nachfolger von Liebig nach München berufen. Er arbeitete u.a. über Phthaleine (Fluorescein 1871), Hydrobenzene, Acetylene, Terpene, Oxoniumsalze und Pyrone. Sein Hauptwerk war die Indigosynthese. Die Kondensation von Phenol und Formaldehyd im Jahre 1872 (Baeyer-Reaktion), war die Grundlage zur Herstellung von Bakelit durch L.H. Beakeland. Bei der Baeyer-Villiger-Oxidation (1899) werden Persäuren zur Oxidation von Ketonen zu Estern eingesetzt. Für seine Verdienste bei der Entwicklung der organischen Chemie wurde Baeyer 1905 mit dem Nobelpreis ausgezeichnet.
*Traugott Sandmeyer (15.9.1845-9.4.1922)
Zunächst machte Sandmeyer eine Lehre als Feinmechaniker in Zürich, wurde 1875 Geselle und machte sich 1877 selbständig. Er erwarb sich autodidaktisch chemische Kenntnisse und wurde 1881 Vorlesungsassistent bei V. Meyer an der ETH. 1888 ging er als wissenschaftlicher Mitarbeiter zur Firma Geigy in Basel, wo er 1901 Direktor und Mitglied des Verwaltungsrates wurde. 1884 findet er die Sandmeyer-Reaktion. In den Jahren 1899 und 1912 publiziert Sandmeyer zwei Verfahren zur Indigoherstellung. Daneben entwickelte er eine Reihe weiterer Farbstoff- und Zwischenprodukteverfahren.
*Karl Heumann (10.9.1850-5.8.1894)
Heumann studierte Chemie an der Technischen Hochschule in Darmstadt und an den Universitäten von Heidelberg und Berlin. Danach war er zunächst Privatdozent in Darmstadt und wurde 1877 Professor für chemische Technologie an der ETH in Zürich. Neben Arbeiten auf anorganischem Gebiet beschäftigte er sich mit Azo- und Diazoverbindungen. Sein Haupterfolg waren die beiden Indigosynthesen 1880.
*Johannes Pfleger (11.9.1867-8.8.1957)
Seit 1891 war Pfleger als Chemiker, später als Chefchemiker bei der Firma Degussa in Frankfurt am Main angestellt. Das von ihm 1901 gefundene Kondensationsmittel Natriumamid verhalf der Heumann-Indigosynthese zum Durchbruch. Es wird daher oft von der Heumann-Pfleger-Indigosynthese gesprochen.
*René Bohn (7.3.1862-6.3.1922)
Studierte Chemie am Polytechnikum in Zürich und schloss 1882 als Dipl-Ing.Chem. ab. 1883 promoviert er bei Heumann. Ab 1884 war er bei der BASF sowohl in der Farbstofforschung wie auch im Färbetechnischen Dienst tätig. 1906 kam er in der Vorstand der BASF. Bohn entwickelte Farbstoffe auf der Basis von Gallussäure, Pyrogallol, Naphthalen und Anthracen. 1889 fand er, dass mit rauchender Schwefelsäure und Quecksilber als Katalysator Hydroxylgruppen in Anthrachinonderivate eingeführt werden können (Bohn-Schmidt-Reaktion). 1901 entdeckte er die Indanthrene (Indigo aus Anthracen), die zu einer der wichtigsten Farbstoffklasse wurden. 1912 erschloss er mit den Chromiumkomplex-Säure-Farbstoffen eine weitere Farbstoffklasse.
Paul Friedländer (29.8.1857-4.9.1923)
Studium der Chemie in Königsberg, Strassburg und München, wo er Assistent bei A. von Baeyer wurde und diesem bei der Indigosynthese zur Seite stand. Die Friedländersche-Chinolinsynthese, die Kondensation von 2-Aminobenzaldehyd mit Carbonylverbindungen, die in Nachbarstellung zur C=O- Gruppe eine reaktionsfähige CH2- Gruppe besitzen, fand er 1882. Beim Versuch 1906 Schwefelfarbstoffe in der Firma Casella aufzuklären, kam ihm die Idee, Thioindigo herzustellen. Er synthetisierte ab 1908 indigoide Verbindungen aller Nuancen. 1909 isolierte er aus Schnecken (Murex brandaris) Purpur und klärte die chemische Konstitution auf.